
案情速览:
美国联邦巡回上诉法院(CAFC)在Amgen Inc. v. Sandoz Inc.案中,维持地区法院'101专利有效的结论,认为涉案优先权文件中记载的Apremilast的合成工艺能够固有的公开Apremilast的B晶型,优先权成立。Sandoz主张的证据由于公开日在优先权日之后申请日之前不属于现有技术(点击下面的阅读原文可阅读判决原文)。该案再一次表明了优先权对于医药专利的重要性。
行业启示:
尽量保证优先权的充分公开和成立,避免“虚假的”优先权日,误导后续专利布局和信息公开的策略。
“固有公开”举证责任在于主张优先权的一方,证明标准极高,非必要应该进行直接披露,而非依靠固有公开推定披露。
专利申请过程中的意见陈述均会作为后续诉讼中的“呈堂证供”,企业IPR应当保证各国意见陈述中的事实和理由一致,避免相互矛盾增加后续诉讼过程中的解释和证明成本。
对于晶型专利的挑战,某些在先公开的制备工艺可能会固有公开晶型,专利挑战者不妨一试。
案件背景:
Otezla(Apremilast,阿普斯特)是一种口服选择性磷酸二酯酶4(PDE4)小分子抑制剂,在美国已批准3个适应症(中重度斑块型银屑病、活动性银屑病关节炎、白塞病相关口腔溃疡)。Otezla是Celgene的一款口服抗炎药,于2019年8月被Amgen以134亿美元收购。Otezla 2024年的销售额约为21.26亿美元。
Sandoz Inc.、Zydus及其他多家仿制药公司提交了ANDA申请,Amgen诉其侵权。Amgen Inc. v. Sandoz Inc.案涉及三项关键美国专利:7,427,638('638专利,涵盖Otezla的活性成分阿普斯特的药物组合物,有效期至2028年8月);7,893,101('101专利,涵盖阿普斯特的结晶形式,有效期至2023年12月);10,092,541('541专利,涵盖阿普斯特的给药方法,有效期至2034年11月)。
Sandoz和Amgen均上诉。美国联邦巡回上诉法院于2023年4月19日维持新泽西地区法院的判决,认定Sandoz和Zydus的仿制药侵犯了Amgen的药物组合物和晶型两项专利。
该判决禁止Sandoz和Zydus在2028年2月之前生产、销售或进口Otezla的仿制药。但仿制药仍可比原预期(2034年)提前6年进入市场。
本文将仅关注'101专利的专利判决,尤其是判决中的对于固有公开的认定。
案件事由:
涉案专利:'101专利,涵盖阿普斯特的结晶形式,保护期至2023年12月。
涉案权利要求:
1. A Form B crystal form of the compound of Formula (I):
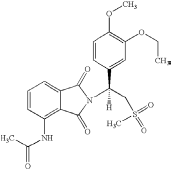
which is enantiomerically pure, and which has an X-ray powder diffraction pattern comprising peaks at about 10.1, 13.5, 20.7, and 26.9 degrees 2θ.
15. A solid pharmaceutical composition comprising the crystal form of any one of claims 1 and 2 to 13.
优先权基础:2002-03-20提交的US临时申请60/366,515('515临时申请),'515 临时申请披露了阿普斯特的化学合成方法,但仅称“得到固体”,未明确晶型。
Sandoz通过'515 临时申请未公开B晶型质疑'101专利的优先权日认定,挑战'101专利的创造性。
争议焦点:
'515临时申请披露的合成方法中是否固有公开了B晶型,使'101专利能够享有该优先权, '515 临时申请不能作为评价'101专利新颖性和创造性的现有技术?
CAFC判决结论和概要:
CAFC认为地区法院认定'101专利享有2002-03-20优先权日并无明显错误;Sandoz未能证明该日期之前的现有技术使权利要求1、15显而易见或丧失新颖性。概要如下:
1、举证责任与标准
主张优先权的一方(Amgen)需证明临时申请必然披露所主张特征;证明标准:固有性要求必须“必然且不可避免”,不能仅凭概率或可能性。
2、认可Amgen复现实验结果
Amgen提供了来源于不同实验室、不同批次的13组复现实验一致得到B晶型的证据,Sandoz未提交任何反例,因此,法院认可Amgen的观点,并认为Sandoz没有证实实施例2能产生B晶型外的其他晶型。
3、Celgene欧洲陈述的排除
法院采纳Amgen的专家证言,C晶型需要甲苯溶剂,甲苯构成C晶型的一部分,认为Celgene向欧专局陈述的“实施例2可以得到C晶型”存在错误。
Q&A
问题:
为什么阿普斯特药物组合物专利(7,427,638,申请日为2005年04月13日,有效期至2028年8月)比晶型专利(7,893,101,申请日为2008年03月27日,有效期至2023年12月)的到期日还晚约5年?
答案:
7,427,638为分案,申请日为2005.04.13,母案申请日为2003.03.19,专利保护期20年,PTE专利期限延长1186天,PTA专利期限延长609天,儿童用药数据独占权6个月。
2003.03.19+20Y+609D+1186D+6M=2028.08.16
7,893,101为分案,申请日为2008.03.27,母案申请日为2003.03.19,专利保护期20年,PTA专利期限延长265天,无PTE延长和儿童用药数据独占权。
2003.03.19+20Y+265D=2023.12.09
可见,尽管两个专利母案申请日相同,专利保护的起算日期相同,由于PTA、PTE、儿童用药数据独占权的不同,专利到期日不同。因此,在计算专利保护期限时,应综合考虑PTA、PTE、儿童用药数据独占权等可能导致专利保护期限延长的因素,避免计算错误。
